Paul Schützenberger (1829-1897) Photomechanical print
Crédit : Wellcome Library, London. Wellcome Images. Licence : CC BY 4.0 Téléchargé sur Wikimedia Commons
Retour sur l’article "Une manufacture de châles imprimés, sur les rives de l’Ohmbach"
Dans l’article mentionné ci-dessus [1], M. Michel expliquait certains termes techniques concernant l’art du teinturier. Quand je lui ai soumis quelques commentaires pour une éventuelle révision, il m’a proposé d’écrire plutôt un court texte à ce sujet. Trois mois plus tard, voici ce texte qui a pris du volume et dont la présence sur obermundat.org pourra surprendre. Mais que le lecteur ne se laisse pas rebuter par la présence de formules chimiques : il ne s’agit nullement d’un cours de chimie. Le texte commente, je l’espère sans trop jargonner, trois notes de l’article initial et se termine par une conclusion qui est en réalité une ouverture sur quelques personnages en relation avec la chimie des couleurs.
Note 3
Citation : "Ce goudron comprend de nombreux hydrocarbures, dont de l’aniline."
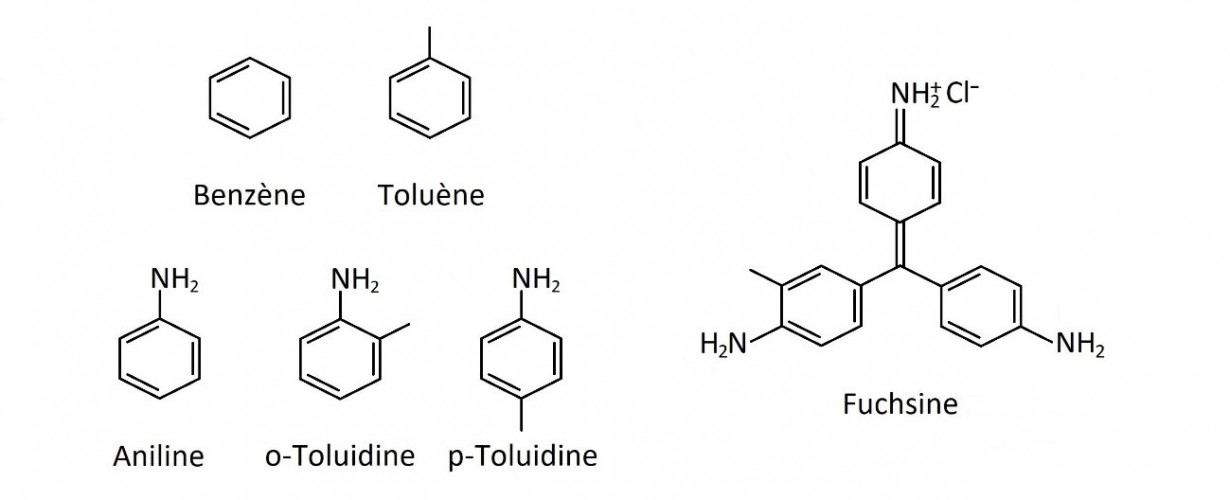
La première partie de la proposition est juste. Par contre, l’aniline n’est pas un hydrocarbure. [2] Sa molécule comporte, en effet, un groupe azoté -NH2 ; de ce fait, elle appartient à la famille des amines. [3]
Schéma 1. La fuchsine est aussi appelée chlorhydrate de rosaniline.
Clés de lecture. Les lignes brisées représentent le squelette carboné des molécules qui est constitué d’atomes de carbone liés entre eux : à chaque angle et à chaque extrémité se trouve un atome de carbone ; chaque segment représente une liaison. Certains atomes de carbone portent un ou plusieurs atomes d’hydrogène qui ne sont pas représentés. Les atomes représentés sont ceux des groupes fonctionnels qui déterminent les propriétés chimiques des molécules. Atomes : C (carbone) ; H (hydrogène) ; O (oxygène) ; N (azote).
Du goudron de houille, qui était le résidu de la distillation de la houille dans les usines à gaz, on tirait, par de nouvelles distillations, de nombreuses matières premières pour la chimie organique. [4] Après la mise en évidence de l’intérêt industriel des "couleurs d’aniline" comme la mauvéine de Perkin (1856), la fuchsine de Verguin (1858) [5] et d’autres à leur suite, l’aniline était devenue une matière première très demandée. Le goudron de houille en renfermait, mais on ne l’en extrayait qu’en trop faible quantité, mélangée à d’autres produits, de sorte que l’on s’est rapidement détourné de cette voie d’accès. La préparation industrielle de l’aniline s’est plutôt orientée vers la transformation du benzène – un hydrocarbure appelé la benzine au XIXe siècle – que l’on isolait imparfaitement du goudron de houille par distillations successives. [6] Ainsi, la plupart des lots de benzène contenaient aussi du toluène. [7] Et leur transformation en "aniline" conduisait en réalité à un mélange de trois produits : de l’aniline formée à partir du benzène et deux toluidines formées à partir du toluène (voir Schéma 1). C’est l’utilisation d’un tel mélange qui a permis la découverte, par un heureux hasard, de la fuchsine dont la molécule résulte de la combinaison de ces trois réactifs.
Cette chimie basée sur la houille s’appelle la carbochimie. A partir du milieu du XXe siècle, elle a été progressivement remplacée par la pétrochimie en même temps que le gaz de ville, produit par les usines à gaz, était remplacé par le gaz naturel.
Note 5
Qu’est-ce que le mystérieux léogomme ?
Le texte cité par M. Michel indique que c’est un épaississant. Les teinturiers utilisaient pour épaissir les couleurs et les mordants, et ainsi leur donner la viscosité adéquate à l’emploi qu’ils comptaient en faire, des gommes végétales naturelles (gomme du Sénégal, gomme adragante…) [8] qui étaient chères. Ils étaient, par conséquent, en demande de substituts d’un prix moins élevé. Le léogomme, que l’on trouve fréquemment sous l’appellation de léiogomme ou de son altération léïocomme, voire léïocome, [9] était l’un d’eux. Il s’agit de fécule de pomme de terre torréfiée. [10] Mais en raison de sa coloration rousse, et de celle de ses solutions dans l’eau, le léiogomme ne convenait que pour épaissir les couleurs foncées et certains mordants.
Il y avait en Alsace, au XIXe siècle, plusieurs producteurs de léiogomme comme Bloch à Duttlenheim [11] et Laederich à Mulhouse .[12]
Note 1
Citation : "L’acide carminique est un éther rouge."
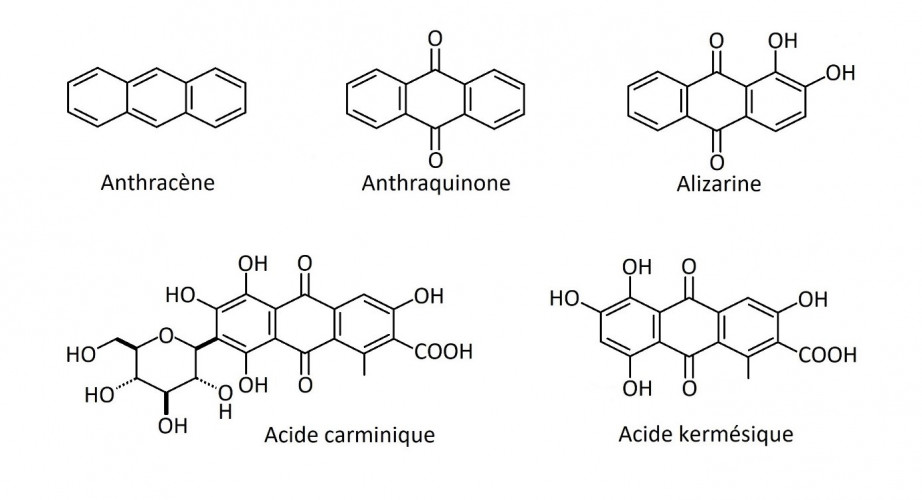
L’acide carminique est surtout… un acide. En effet, sa molécule porte un groupe –COOH caractéristique des acides carboxyliques. [13] Bien qu’elle comporte aussi d’autres groupes : –OH, >C=O et un enchainement >CH-O-CH< caractéristique d’un éther [14] dans le cycle (l’hexagone) le plus à gauche (Schéma 2), les règles compliquées de nomenclature de la chimie organique prévoient que le groupe –COOH a priorité sur tous les autres ; par conséquent la molécule est appelée un acide.[ 15]
De plus, la couleur rouge de l’acide carminique est due, non pas au groupe éther, mais aux trois cycles de droite et aux groupes qu’ils portent. Ces trois cycles forment une anthraquinone c’est-à-dire une quinone dérivée de l’anthracène.
Schéma 2.
D’autres composés rouges comme l’acide kermésique et l’alizarine ont également une structure anthraquinonique.
Depuis l’Antiquité on tirait un colorant rouge à base d’acide kermésique [16] de la cochenille Kermes vermilio, un insecte du bassin méditerranéen. [17] Mais à partir du XVIe siècle, après la découverte de l’Amérique, il a été progressivement supplanté par le colorant provenant de la cochenille du Mexique Dactylopius coccus, celui qui contient l’acide carminique. Quant à l’alizarine, il s’agit du constituant majeur du colorant extrait de la garance, une plante tinctoriale connue depuis l’Antiquité et cultivée, notamment en Alsace aux XVIIIe et XIXe siècles, jusqu’à ce que le produit naturel soit supplanté par l’alizarine de synthèse, moins chère.
C’est aussi l’évolution vers l’utilisation de colorants de synthèse qui a conduit la manufacture d’extraits de bois tinctoriaux Roesler, fondée en 1870 à Dornach près de Mulhouse, à s’orienter dans les années 1890 vers la fabrication d’aniline à partir de benzène et à construire à cette fin une nouvelle fabrique. Par la suite, elle étendra sa production à d’autres intermédiaires et à d’autres domaines et poursuivra ses activités sur le même site jusqu’en 2007 sous plusieurs dénominations 18]
En guise de conclusion
L’année même de la création de la manufacture de châles de Rouffach, en 1867 donc, a été publié le "Traité des matières colorantes" de Paul Schützenberger, "sous les auspices de la Société Industrielle de Mulhouse et avec le concours de son Comité de chimie" est-il précisé. [19] Le chimiste – et médecin – alsacien y décrit, en deux tomes et près de 1200 pages, l’état de l’art à cette époque. Docteur ès sciences physiques depuis 1863, Schützenberger [20] avait rejoint en 1865 le laboratoire de Balard au Collège de France après avoir, pendant onze ans, enseigné la chimie à l’Ecole supérieure des sciences de Mulhouse. [21] On trouve dans ce traité tous les termes mentionnés dans l’article de M. Michel : couleurs d’aniline, cochenille, bois de campêche, fustel (appelé fustet), léogomme (appelé léïocome, au féminin) et aussi mordants qui désignent les composés chimiques permettant l’accrochage des couleurs sur les textiles. Schützenberger poursuivra à Paris une belle carrière en ayant toujours le souci des applications industrielles de la science et de leur transmission : devenu professeur au Collège de France, il sera le premier directeur et l’organisateur de l’Ecole de physique et de chimie industrielles de la ville de Paris [22] – l’actuelle ESPCI Paris – dont la création avait été proposée dès 1878 par Charles Lauth [23] pour compenser la perte, après la guerre de 1870, de l’école de Mulhouse dans laquelle Schützenberger avait enseigné.
Denis Heissler
Références bibliographiques et notes
[1] G. Michel. "Une manufacture de châles imprimés, sur les rives de l’Ohmbach". Obermundat.org [En ligne]. Publié le 7 septembre 2022.
[2] Un hydrocarbure est un composé dont la molécule est formée exclusivement d’atomes de carbone et d’hydrogène. L’hydrocarbure le plus simple est le méthane CH4 qui est un gaz à 25 °C et à pression atmosphérique. Dans les mêmes conditions, le benzène C6H6 est un liquide et l’anthracène C14H10 est un solide.
[3] Le groupe -NH2 consiste en un atome d’azote N (N pour nitrogène) lié à deux atomes d’hydrogène H. Dans les documents français du XIXe siècle, l’azote est noté Az.
[4] La chimie organique est la chimie des composés du carbone. De nombreuses molécules carbonées entrent dans la constitution et sont nécessaires au fonctionnement des organismes vivants.
[5] M. Chastrette. "La découverte de la fuchsine." L’actualité chimique, 2009, n° 333, p. 48-53. L’article, accessible sur internet, décrit notamment les débuts industriels agités de la fuchsine.
[6] L’aniline était produite par nitration du benzène puis réduction du nitrobenzène intermédiaire C6H5NO2. (Noter que de nombreux composés issus du goudron de houille dont le benzène, l’aniline et les toluidines sont cancérigènes). Pour la transformation du benzène en aniline, voir par exemple : (a) P. Bolley et E. Kopp. "Traité des matières colorantes artificielles dérivées du goudron de houille". Librairie F. Savy - Paris ; 1874 ; p. 79 (nitration) et p. 123 (réduction) ; (b) A. Wurtz. "Progrès de l’industrie des matières colorantes artificielles". G. Masson, éditeur - Paris ; 1876 ; p. 48 (nitration) et p. 49 (réduction). Source pour les deux ouvrages : gallica.bnf.fr / Bibliothèque nationale de France. (Pour E. Kopp, voir aussi Réf. 26 ; pour A. Wurtz, voir aussi Réf. 24).
[7] Pour la description de l’obtention de différentes qualités de benzène, voir Réf. 6b, p. 28-32. Et aussi Réf. 6a, p. 24 (milieu de la page) et pages suivantes.
[8] La gomme du Sénégal (variété dure de gomme arabique) et la gomme adragante sont des exsudats solidifiés d’arbustes : divers Acacias d’Afrique sahélienne pour la première, divers Astragalus du sud de la région ponto-caspienne pour la seconde.
[9] Larive et Fleury. "Dictionnaire français illustré des mots et des choses." Tome 2. G. Chamerot, imprimeur-éditeur - Paris ; 1889 ; p. 283. Source : gallica.bnf.fr / Bibliothèque nationale de France. (Larive et Fleury sont des pseudonymes sans prénoms).
[10] (a) Ch.-E. Guignet, F. Dommer, E. Grandmougin. "Industries textiles : blanchiment et apprêts, teinture et impression, matières colorantes." Gauthier-Villars et Fils - Paris ; 1895. p. 336 ; (b) L. F. Dubief. "Guide pratique du féculier et de l’amidonnier." 2e Edition. E. Lacroix, éditeur - Paris ; 1865 ; p. 188-192. Source pour les ouvrages (a) et (b) : gallica.bnf.fr / Bibliothèque nationale de France ; (c) Réf. 19, Tome 1, p. 89.
[11] (a) S. Bottin. "Almanach-Bottin du commerce de Paris, des départements de la France et des principales villes du monde." Paris ; 1842 ; 45e année ; p. 889. Source : gallica.bnf.fr / Bibliothèque nationale de France ; (b) Duttlenheim se trouve dans le Bas-Rhin, entre Strasbourg et Molsheim.
[12] R. Oberlé. "Laederich." Nouveau dictionnaire de biographie alsacienne ; FSHAA ; 1994. Notice disponible sur NetDBA (www.alsace-histoire.org/netdba/laederich/)
[13] Le groupe –COOH consiste en un atome de carbone C lié à deux atomes d’oxygène O dont l’un porte un atome hydrogène H.
[14] Aujourd’hui, on appelle éther un composé comportant un enchainement C-O-C dans sa structure. Exemple : l’éther vendu en pharmacie CH3-CH2-O-CH2-CH3. Autrefois, on appelait ces composés éthers-oxydes pour les distinguer des éthers-sels, les actuels esters.
[15] Les règles de nomenclature sont établies par l’Union internationale de chimie pure et appliquée souvent désignée par son acronyme anglais : IUPAC.
[16] On remarque que l’acide kermésique est identique à une partie de l’acide carminique. (Pour les amateurs de chimie, le premier est l’aglycone du second qui est un C-aryl glycoside.)
[17] (a) D. Cardon. "La garrigue, monde de l'écarlate." Études rurales. 1999 ; n°151-152, Autres temps, autres lieux ; p. 33-42. (www.persee.fr/doc/rural_0014-2182_1999_num_151_1_4114) ; (b) C. Joliot, C. Mathe de Souza, C. Vieillescazes. "Inventaire scientifique de la pharmacie de l’ancien Hôpital Sainte Marthe d’Avignon". 2018 ; p. 119-124. Identifiant sur internet : hal-01775007.
[18] "Roesler" (Les Roesler, industriels à Dornach) et "ICMD-115 ans" (Un peu d’histoire), deux documents téléchargeables sur le site de la Mémoire Mulhousienne consulté le 14 décembre 2022 (www.memoire-mulhousienne.fr/cimetiere-de-dornach.html)
[19] P. Schützenberger. "Traité des matières colorantes comprenant leurs applications à la teinture et à l'impression et des notices sur les fibres textiles, les épaississants et les mordants." Tomes 1 et 2. V. Masson et Fils - Paris ; 1867. Source : Cnum – Conservatoire numérique des Arts et Métiers – (cnum.cnam.fr)
[20] Paul Schützenberger (Strasbourg 1829 - Mézy-sur-Seine 1897). Voir sa biographie, classée sous la lettre P, initiale de son prénom, sur le site de la Société chimique de France (new.societechimiquedefrance.fr/produit_du_jour/)
[21] En 1822, le collège municipal de Mulhouse ouvre un cours de chimie appliquée aux arts, incluant des travaux pratiques, avec le concours de plusieurs industriels du textile qui avaient besoin de chimistes. En 1855, un an après que Schützenberger ait commencé à y enseigner, le cours est rattaché à l’Ecole supérieure des sciences de Mulhouse. Par la suite, à travers de multiples évolutions, cette formation a conduit à l’actuelle Ecole nationale supérieure de chimie de Mulhouse. (Source : www.enscmu.uha.fr ; onglet "200 ans de chimie" puis "Histoire et patrimoine" puis document téléchargeable "Archives historiques de l’ENSCMu." Consulté le 23 nov. 2022)
[22] (a) Schutzenberger est directeur de l’Ecole parisienne de 1882 à 1897. Ses successeurs immédiats sont les chimistes alsaciens Charles Lauth (de 1898 à 1904) et Albin Haller (de 1905 à 1924) ; (b) Ch. Lauth. "Rapport général sur l’historique et le fonctionnement de l’École municipale de physique et de chimie industrielles." Ville de Paris - Paris ; 1900. (Source : www.espci.psl.eu/fr/espci-paris-psl/bibliotheque/ ; aller sur "Centre de ressources historiques" puis "Ouvrages et documents." Consulté le 16 nov. 2022) ;
(c) En 1896, le chimiste alsacien Charles Friedel (Réf. 24) fonde et dirige le Laboratoire de chimie pratique et industrielle qui évoluera pour devenir l’actuelle Ecole nationale supérieure de chimie de Paris. Friedel était alors professeur de chimie organique à la Sorbonne où il avait succédé à son maître Wurtz (Réf. 24), un autre alsacien ; (d) Le successeur de Friedel à la Sorbonne est Haller (Réf. 25), qui avait auparavant initié la fondation puis assuré la direction de l’Institut chimique de Nancy devenu l’actuelle Ecole nationale supérieure des industries chimiques de cette ville. Toutes ces personnalités avaient le souci de former des ingénieurs-chimistes pour l’industrie, conscients qu’ils étaient du retard qu’avait pris la France dans ce domaine.
[23] Charles Lauth (Strasbourg 1836 - Nice 1913) a travaillé pour l’industrie des colorants (plusieurs inventions dont le violet de Lauth). Il a aussi été administrateur de la Manufacture nationale de Sèvres de 1879 à 1887 où son successeur a été le céramiste Théodore Deck (Guebwiller 1823 - Sèvres 1891). Pour une biographie : V. Beyer, J.-M. Schmitt. "Lauth". Nouveau dictionnaire de biographie alsacienne ; FSHAA ; 1994. Notice disponible sur NetDBA (www.alsace-histoire.org/netdba/lauth/)
24 Charles Friedel (Strasbourg 1832 - Montauban 1899) ; Charles-Adolphe Wurtz (Strasbourg 1817 - Paris 1884). Voir leurs biographies, classées sous la lettre C, initiale de leurs prénoms, sur le site de la Société chimique de France (new.societechimiquedefrance.fr/produit_du_jour/)
25 Albin Haller (Fellering 1849 - Paris 1925) ; P. Labrude. "Albin Haller (1849-1925), pharmacien et chimiste". Revue d’histoire de la pharmacie. 1982 ; 70ᵉ année ; n° 254 ; p. 207-209. (www.persee.fr/doc/pharm_0035-2349_1982_num_70_254_2615).
26 Charles-Emile Kopp (Wasselonne 1817 - Zurich 1875), co-auteur de l’ouvrage cité en Réf. 6a ; J. M. Chézeau. "Émile Kopp, chimiste et homme politique alsacien méconnu." L’actualité chimique, 2018, n° 435, p. 43-47. Accessible sur internet.
Droit d'auteur et propriété intellectuelle
L'ensemble de ce site relève de la législation française et internationale sur le droit d'auteur et la propriété intellectuelle. Tous les droits de reproduction sont réservés. Toute utilisation d'informations provenant du site obermundat.org doit obligatoirement mentionner la source de l'information et l'adresse Internet du site obermundat.org doit impérativement figurer dans la référence.